- Hot Line:
+(86)15801695345 - E-mail:
nar@china-reach.net

中国化粧品の登記サービス|新安潤コンサルティング株式会社
化粧品の新原料の備案/登録

化粧品の新しい原料の定義:化粧品の新しい原料は、化粧品の生産に国内で初めて使用される天然または人工の原料を指します。
実施許可の法的根拠:化粧品衛生監督規則、化粧品衛生監督規則の実施規則、健康関連製品の衛生管理許可手続き、化粧品行政許可の申告及び受理に関する規定、化粧品行政許可の受理及び審査の要点
所轄官庁:国家食品医薬品局の受付場所:国家食品医薬品局管理受付サービスセンター
異なる状況で化粧品の新しい原料規制規制要件
| 状況 1 | 状況2 | 状況3 |
| 原料は中国で化粧品の新しい原料です | 原料は中国で新しい化学物質です | この原料は、中国では化粧品の新しい原料と新しい化学物質の両方に属しています |
| 化粧品の新しい原料が中国の既存の化学物質リストにあるが、中国で承認されていない化粧品原料のカタログにある場合は、国家食品医薬品局(FDA)で化粧品の新しい原料の管理許可を取得する必要があります。 | 新しい原料が中国で承認されている化粧品原料のカタログで、中国の既存の化学物質リストに含まれている場合は、中国環境保護省に新化学物質登録証明書を申請する必要があります。 | 化粧品新素材製造企業は、企業自身の状況に応じて、国家食品医薬品局と中国環境保護省に申請し、化粧品新原料管理許可、新化学物質登録証明書を処理した後、中国市場で販売することができます。 |
一、適用範囲
国内中華人民共和国で生産・運営されている化粧品の新素材
二、政策と規制
1、化粧品監督管理規則(中華人民共和国国務院令第727号)
コンテンツリンク:https://www.nmpa.gov.cn/xxgk/fgwj/flxzhfg/20200629190501801.html
コンテンツリンク:https://www.nmpa.gov.cn/xxgk/fgwj/flxzhfg/20210112114521164.html
3、化粧品新素材登録記録資料管理規定
コンテンツリンク:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20210304140454159.html
4、化粧品登録記録資料管理規定
コンテンツリンク:https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20210304140747119.html
三、備案/登録プロセス
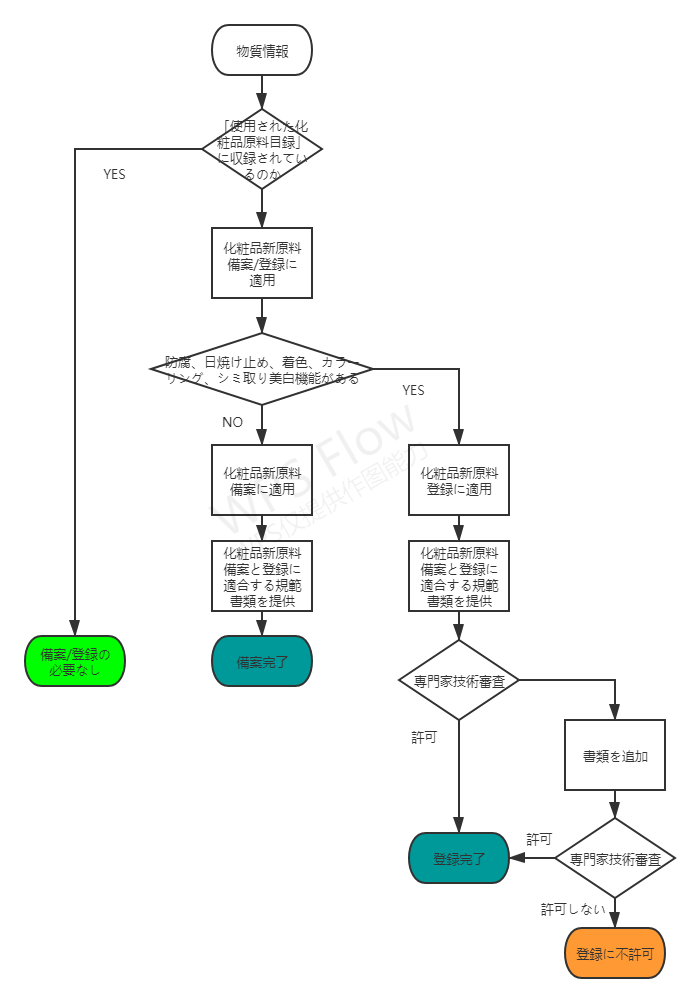
四、情報要件
1、化粧品新原料の備案/登録申請フォーム
2、新原料開発レポート
3、新しい原料の調製プロセス、安定性、品質管理基準などの研究資料
4、新しい原料の安全性評価データ
五、サービス内容
1、化粧品原料の品質と安全性に関する情報の配信サービス
2、化粧品新原料理化/毒物学/効能などの試験監理サービス
3、化粧品新素材安全評価サービス
4、化粧品の新しい原料の備案/登録プロセス全体を追跡します
化粧品原料情報の報告
一、規制の背景
「化粧品登録記録データ基準」(草案、2020/11/4)第27条(二)は、「登録者、記録者、または国内責任者は、製品に使用される原材料の製造業者情報を記入し、原材料メーカーが発行する原材料品質安全情報文書をアップロードしなければならない」と規定しています。 原材料の製造業者が「化粧品原料の品質と安全に関する情報の提出に関するガイドライン」(附属書12および附属書13)に従って原材料の品質と安全性に関する情報を提出した場合、登録者、記録者、または国内責任者は、原材料の品質安全に関する情報文書(附属書14)に記入することができます。
二、報告プロセス
1. 既存原料及び化粧品新原料の判定を行う
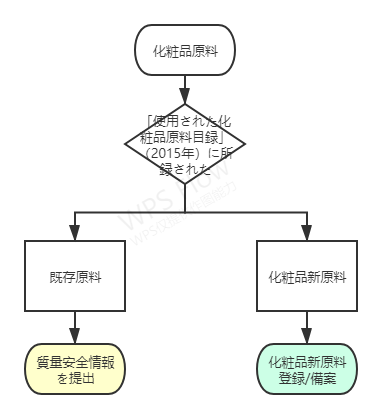
図1 「使用した化粧品原料目録」(2015年版)に基づいて、既存原料及び化粧品新原料の判定
2. 化粧品登録における原料の品質と安全性に関する情報管理
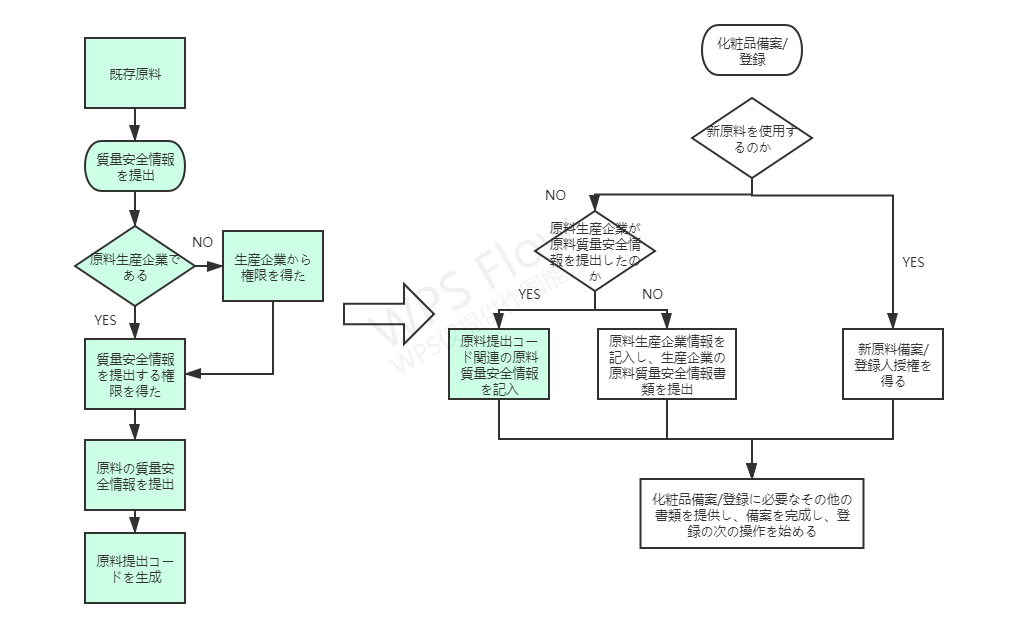
図2 化粧品登録における原料品質安全情報管理
三、公式の化粧品原料安全性情報報告ガイドライン
(A)化粧品原料メーカーとは、原料の安全に責任を負う企業であり、原料の実際生産企業、原料の実際の生産企業と同一グループ会社に属する関連企業又は原料委託生産行為における委託企業であってもよい。
化粧品原料メーカーは、国家薬物管理局の原料安全情報サービスプラットフォームを通じて、「原料安全関連情報備案企業情報表」と企業登記証明書を提出する必要があり、化粧品原料安全関連情報報告権限を開通します。
(B)海外または国内の原材料メーカーは、独自で化粧品原料の安全性情報を提出することができ、国外又は国内法人企業に原料安全情報の報告と日常メンテナンスを授権することができます。授権された企業がユーザー権限を開通する際、化粧品原料メーカーが発行した授権書も同時に提出しなければならない。授権書は授権関係と授権範囲を明確にし、同じ品質規格の原料安全関連情報は1つの企業にしか授権できない。
(C)原材料の安全性関連情報は、原材料の商品名、原材料の基本情報、生産工程の簡単な説明、必要な品質管理の要件、国際権威機関の評価結論、リスク物質の制限要件などを含める必要があります。
化粧品の生産用水は、原材料の安全性に関連する情報を報告する必要はありませんが、特殊な産地の出所用水を除きます。
(D) 原料安全に関する情報は情報プラットフォームを通じて提出された後、自動的に原料報告コードが生成されます。原料報告コードは5つのメーカーデジタルコード、6つの原料デジタルコードと3つの原料品質規格デジタルコードから構成され、各グループのコード間は「-」で接続されています。
(E)国家薬品監督管理局は原料安全情報を報告した原料商品名、生産者情報と原料報告コードを公開します。
化粧品登録者、備案人または国内責任者は、特殊化粧品登録を申請したり、普通化粧品届出を行ったりする際に、原料報告コードを記入し、原料安全情報書類と関連をつけます。原料メーカー、安全関連情報が変更された場合、登録者、備案人または国内責任者は直ちに関連資料を変更しなければならない。
四、原料情報報告の過渡期政策
NMPA は、関連する経過措置を策定し、原材料コードを報告する必要な情報を決定しました。化粧品会社は、過渡期政策に従って事前準備を行う必要があります。
2021年5月1日以降、登録者/届出人が登録を申請したり、届出を行ったりする際に、「化粧品安全技術規範」で品質規格が求められている原料を含み、製品の製剤に使用されている成分の出所・商品名に関する情報を記入し、成分の品質規格または安全性に関する証明も提出しなければならない。
2022年1月1日以降、登録者/届出人が登録を申請したり、届出を行ったりする際に、「規定」の要求に従い、防腐、日焼け止め、着色、染髪、シミ取り美白機能を有する原料の安全に関する情報を提供しなければならない。
2023年1月1日以降、登録者/届出人が登録を申請したり、届出を行ったりする際に、「規定」の要求に従い、すべての原料の安全に関する情報を提供しなければならない。これまで登録を取得したり、登録を完了したりした化粧品は、登録者/届出者は2023年5月1日までに製品配合物のすべての原料の安全に関する情報を追加補充しなければならない。
五、原料メーカー及び化粧品メーカーの対応策
(1) 化粧品原料企業
できるだけ早く下流の化粧品企業の製品の登録を容易にするために提出された原材料の品質と安全性の情報を完了します。新制度では、化粧品の申請・登録の際に、原材料の品質安全性情報/報告コードを同時に提供する必要があります。
(2)化粧品完成品事業者
既存の原材料在庫を整理し、異なる原材料メーカーが同じ原料を生産する場合、後続の新しい規制要件を満たすには、必要に応じて社内の原材料システムまたは原材料コードを整理する必要があります。 新しい規制では、化粧品備案登録する際に原材料メーカーに直接関連付けられ、申請後に原材料メーカーを変更する必要がある場合は、登録プラットフォームを通じて原材料情報をメンテナンスし、必要に応じて安全性評価を行う必要があります。
化粧品完成品の登録
一、一般化粧品の備案
備案のための一般的な化粧品の輸入:
規制の下では、香港、マカオ、台湾を含む海外から国内市場に輸入されたすべての化粧品は、医薬品局の備案とライセンスを通過し、輸入非特殊化粧品の備案証明書を取得する必要があります。
国産一般化粧品の備案:
規制によると、すべての国内非特殊化粧品は、国家食品医薬品局の承認を得て、国内非特殊化粧品の備案証明書を取得する必要があり、そうでなければ、販売のために市場に出回るか、厳しい罰則に直面しています。
歯磨き粉の備案:
中国国務院は、2021年1月1日から施行される化粧品監督管理規則を公表した。 これは、化粧品衛生監督条例の30年間の改正と更新です。 規制は、通常の化粧品の管理に歯磨き粉を組み込むことは注目に値します。 歯科教育記録者は、国家基準および業界標準に従って有効性評価を行った後、歯科教育は、抗インディゴ、プラーク抑制、抗歯質感受性、歯肉問題の軽減などの効果を有すると主張することができる。 具体的な管理措置は、国務院の医薬品監督管理部門が策定し、国務院の市場監督管理部門に提出し、審査及び公表する。
二、特別な化粧品の登録
輸入特殊化粧品登録:
規制の下では、香港、マカオ、台湾を含む海外から国内市場に販売されているすべての化粧品は、医薬品局のファイリングとライセンスを通過し、輸入特殊化粧品のライセンス承認を取得する必要があります。
国産特殊化粧品登録:
規制によると、すべての国内生産特殊化粧品は、国家食品医薬品局の承認を得て、ライセンスバッチを取得し、販売するために市場に出回るか、または厳しい罰則に直面する必要があります。

 中文
中文 English
English
