- Hot Line:
+(86)15801695345 - E-mail:
nar@china-reach.net

еҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«гҒЁгҒҜгҖҒдё»гҒ«еҢ»зҷӮж©ҹеҷЁгҒ®еҺҹжқҗж–ҷгҖҒйғЁе“ҒгҖҒиЁӯиЁҲгҖҒиЈҪйҖ е·ҘзЁӢгҖҒжҖ§иғҪи©ҰйЁ“гҖҒиҮЁеәҠи©ҰйЁ“гғҮгғјгӮҝеҸҠгҒігҒқгҒ®д»–гҒ®йҮҚиҰҒгҒӘжҠҖиЎ“жғ…е ұгӮ’еҗ«гӮҖжҠҖиЎ“ж–ҮжӣёгҒ§гҒӮгӮӢгҖӮеҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«гҒ®зҷ»йҢІгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгҒ®гӮӨгғҺгғҷгғјгӮ·гғ§гғігӮ’дҝғйҖІгҒ—гҖҒзҷ»йҢІгғ—гғӯгӮ»гӮ№гӮ’з°Ўзҙ еҢ–гҒ—гҖҒгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«жүҖжңүиҖ…гҒ®зҹҘзҡ„иІЎз”ЈжЁ©гӮ’дҝқиӯ·гҒҷгӮӢгҒ“гҒЁгӮ’зӣ®зҡ„гҒЁгҒ—гҒҰгҒ„гӮӢгҖӮ
- еҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІдәӢй …йҒ©з”ЁиҰҸе®ҡ
- еӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҢзҷәиЎЁгҒ—гҒҹеҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІгҒ«й–ўгҒҷгӮӢдәӢй …
- гҖҢеҢ»зҷӮж©ҹеҷЁзҷ»йҢІз®ЎзҗҶејҒжі•гҖҚ
- гҖҢдҪ“еӨ–иЁәж–ӯи©Ұи–¬зҷ»йҢІз®ЎзҗҶејҒжі•гҖҚ
- гҖҢеҢ»зҷӮж©ҹеҷЁзҷ»йҢІгҒ®иҰҒ件гҒҠгӮҲгҒіжүҝиӘҚиЁјжҳҺжӣёйЎһгғ•гӮ©гғјгғһгғғгғҲгҖҚ
- гҖҢдҪ“еӨ–иЁәж–ӯз”Ёи©Ұи–¬зҷ»йҢІз”іе‘Ҡжғ…е ұиҰҒ件еҸҠгҒіжүҝиӘҚиӘҚиЁјж–Үжӣёгғ•гӮ©гғјгғһгғғгғҲгҖҚ
- еҢ»зҷӮж©ҹеҷЁзҷ»йҢІз”іи«ӢжӣёгҒ®йӣ»еӯҗжҸҗеҮәгҒ«й–ўгҒҷгӮӢжҠҖиЎ“гӮ¬гӮӨгғүгғ©гӮӨгғі
- еҝңз”ЁеҲҶйҮҺгҒ«гҒҠгҒ‘гӮӢеҢ»зҷӮж©ҹеҷЁзҷ»йҢІгҒ®еҜ©жҹ»гӮ¬гӮӨгғүгғ©гӮӨгғі
- еҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІдәӢй …гҒ®йҒ©з”ЁзҜ„еӣІ
еҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«гҒ®еҶ…е®№гҒҜгҖҒдё»гҒ«еҢ»зҷӮж©ҹеҷЁгҒ®еҺҹжқҗж–ҷгҖҒйғЁе“ҒгҖҒиЁӯиЁҲгҖҒиЈҪйҖ е·ҘзЁӢгҖҒжҖ§иғҪи©ҰйЁ“гҖҒиҮЁеәҠз ”з©¶гғҮгғјгӮҝгҒҢеҗ«гҒҫгӮҢгӮӢгҖӮ
еҢ»зҷӮж©ҹеҷЁзҷ»йҢІз”іи«ӢиҖ…гҒҢијёе…Ҙ2йЎһгҖҒ3йЎһеҸҠгҒіеӣҪеҶ…3йЎһеҢ»зҷӮж©ҹеҷЁпјҲдҪ“еӨ–иЁәж–ӯи©Ұи–¬гӮ’еҗ«гӮҖпјүгҒ®зҷ»йҢІгҖҒеӨүжӣҙгҖҒиҮЁеәҠи©ҰйЁ“жүҝиӘҚгҒӘгҒ©гҒ®з”іи«ӢдәӢй …гҒ®дёӯгҒ§еј•з”ЁгҒ—гҒҹдё»гҒӘж–ҮжӣёгҒҜгҖҒеҗ„зңҒгҖҒиҮӘжІ»еҢәгҖҒзӣҙиҪ„еёӮи–¬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҢе®ҹйҡӣгҒ®зҠ¶жіҒгҒ«еҹәгҒҘгҒ„гҒҰе…¬е‘ҠгӮ’еҸӮз…§гҒ—гҒҰеӣҪеҶ…2йЎһеҢ»зҷӮж©ҹеҷЁгҒ®дё»гҒӘж–Үжӣёзҷ»йҢІдәӢй …гӮ’еұ•й–ӢгҒҷгӮӢгҖӮ
- еҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІгғ—гғӯгӮ»гӮ№
еӣҪ家薬зӣЈеұҖеҢ»зҷӮж©ҹеҷЁжҠҖиЎ“еҜ©жҹ»гӮ»гғігӮҝгғјгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІгғ—гғ©гғғгғҲгғ•гӮ©гғјгғ гҒЁгғҮгғјгӮҝгғҷгғјгӮ№гӮ’ж§ӢзҜүгҒ—гҖҒгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«гҒ®жүҖжңүиҖ…гҒҜгҖҒиҰҒ件гҒ«еҹәгҒҘгҒ„гҒҰгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІжғ…е ұгӮ’жҸҗеҮәгҒ—гҖҒзҷ»йҢІеҫҢгҒ«гғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІз•ӘеҸ·гӮ’еҸ–еҫ—гҒҷгӮӢгҖӮеҢ»зҷӮж©ҹеҷЁеҜ©жҹ»гӮ»гғігӮҝгғјгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁзҷ»йҢІй–ўйҖЈз”іи«ӢгҒЁй–ўйҖЈгҒ—гҖҒгғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«жғ…е ұгӮ’еҜ©жҹ»гӮ’иЎҢгҒҶгҖӮ
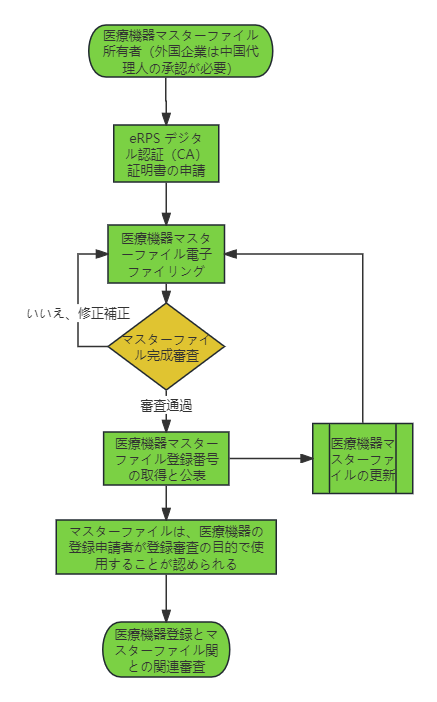
4.гӮөгғјгғ“гӮ№еҶ…е®№
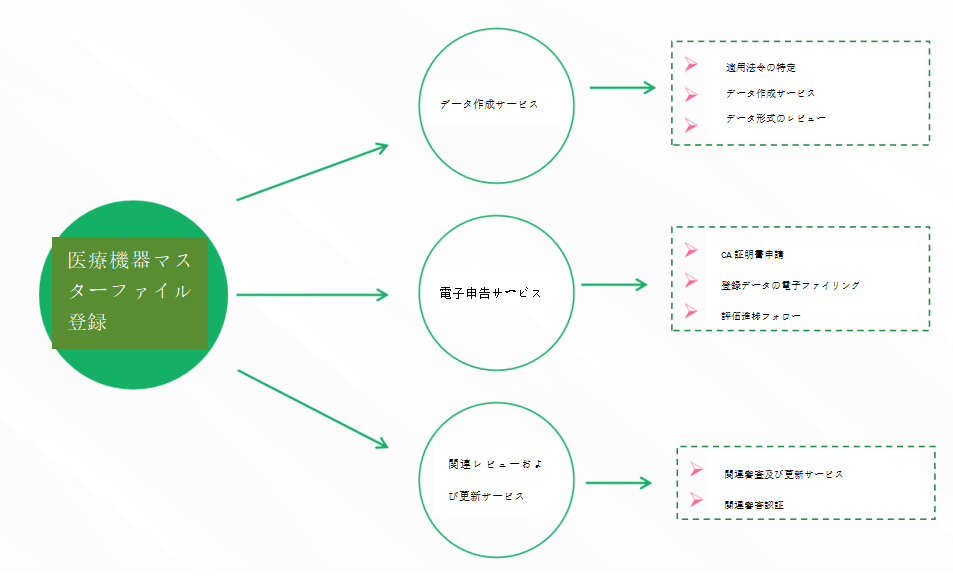
NMPAд»ЈиЎҢгӮөгғјгғ“гӮ№гҖҒePRS CAиЁјжҳҺжӣёз”іи«ӢгҖҒжҠҖиЎ“ж–ҮжӣёдҪңжҲҗгҒҫгҒҹгҒҜгӮ¬гӮӨгғҖгғігӮ№дҪңжҲҗгҖҒзҷ»йҢІз”іе‘ҠгҖҒиЁјжҳҺжӣёгғЎгғігғҶгғҠгғігӮ№гҒӘгҒ©гҖҒгҒҠе®ўж§ҳгҒ®гғһгӮ№гӮҝгғјж–Үжӣёзҷ»йҢІз”іи«ӢгҒ®е…Ёгғ—гғӯгӮ»гӮ№гӮ’д»ЈиЎҢгҒҷгӮӢгҖӮ
- еҢ»зҷӮж©ҹеҷЁиҰҸеҲ¶еҲ¶еәҰгҒ®зҙ№д»Ӣ
еҢ»зҷӮж©ҹеҷЁиҰҸеҲ¶еҲ¶еәҰгҒҜгҖҒдёҖйҖЈгҒ®жі•еҫӢгҖҒиҰҸеҲ¶гҖҒеҹәжә–гҖҒгӮ¬гӮӨгғүгғ©гӮӨгғігҒ§ж§ӢжҲҗгҒ•гӮҢгҖҒгҒ“гӮҢгӮүгҒҢдёҖдҪ“гҒЁгҒӘгҒЈгҒҰгҖҒз ”з©¶й–ӢзҷәгҖҒиЈҪйҖ гҖҒиІ©еЈІгҖҒдҪҝз”ЁгҒ®е…ЁйҒҺзЁӢгҒ«гҒҠгҒ‘гӮӢеҢ»зҷӮж©ҹеҷЁгҒ®иҰҸеҲ¶гҒ®еҹәзӨҺгҒЁгҒӘгҒЈгҒҰгҒ„гӮӢгҖӮ еҢ»зҷӮж©ҹеҷЁиҰҸеҲ¶еҲ¶еәҰгҒҜдё»гҒ«д»ҘдёӢгҒ®гғ¬гғҷгғ«гҒ®иҰҸеҲ¶гҒ§ж§ӢжҲҗгҒ•гӮҢгҒҰгҒ„гӮӢпјҡ
- гҖҢеҢ»зҷӮж©ҹеҷЁзӣЈзқЈз®ЎзҗҶжқЎдҫӢгҖҚ
еҢ»з–—еҷЁжў°зӣ‘з®Ўзҡ„еҹәжң¬жі•и§„пјҢз”ұеӣҪеҠЎйҷўеҸ‘еёғпјҢж¶өзӣ–дәҶеҢ»з–—еҷЁжў°зҡ„еҲҶзұ»гҖҒжіЁеҶҢгҖҒз”ҹдә§гҖҒз»ҸиҗҘгҖҒдҪҝз”ЁгҖҒзӣ‘зқЈз®ЎзҗҶе’Ңжі•еҫӢиҙЈд»»зӯүж–№йқўпјҢдёәеҢ»з–—еҷЁжў°зҡ„зӣ‘з®ЎжҸҗдҫӣдәҶжі•еҫӢдҫқжҚ®гҖҖеӣҪеӢҷйҷўгҒҢзҷәеёғгҒ—гҒҹеҢ»зҷӮж©ҹеҷЁгҒ®зӣЈзқЈз®ЎзҗҶгҒ®еҹәжң¬жі•иҰҸгҒҜгҖҒеҢ»зҷӮеҷЁжқҗгҒ®еҲҶйЎһгҖҒзҷ»йҢІгҖҒз”ҹз”ЈгҖҒзөҢе–¶гҖҒдҪҝз”ЁгҖҒзӣЈзқЈз®ЎзҗҶгҖҒжі•зҡ„иІ¬д»»гҒӘгҒ©гӮ’гӮ«гғҗгғјгҒ—гҒҰгҒҠгӮҠгҖҒеҢ»зҷӮеҷЁжқҗиҰҸеҲ¶гҒ®жі•зҡ„ж №жӢ гҒЁгҒӘгҒЈгҒҰгҒ„гӮӢгҖӮ
- гҖҢеҢ»зҷӮж©ҹеҷЁзҷ»йҢІз”іи«Ӣз®ЎзҗҶејҒжі•гҖҚ
гҖҢеҢ»зҷӮж©ҹеҷЁзҷ»йҢІз”іи«Ӣз®ЎзҗҶејҒжі•гҖҚгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгҒ®зҷ»йҢІз”іи«Ӣгғ—гғӯгӮ»гӮ№гҒ«гҒӨгҒ„гҒҰи©ізҙ°гҒ«иҰҸе®ҡгҒ—гҒҰгҒҠгӮҠгҖҒзҷ»йҢІеҢәеҲҶгҖҒз”іи«ӢиҰҒ件гҖҒжҠҖиЎ“еҜ©жҹ»гҖҒиҮЁеәҠи©ҰйЁ“иҰҒ件гҖҒе„Әе…ҲжүҝиӘҚжүӢз¶ҡгҒҚгҖҒзҷ»йҢІеӨүжӣҙгҖҒзҷ»йҢІз¶ҷз¶ҡгҒӘгҒ©гҒ®еҶ…е®№гҒҢеҗ«гҒҫгӮҢгӮӢгҖӮ
- еӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒ®е…¬е‘ҠгҒЁгӮ¬гӮӨгғүгғ©гӮӨгғіпјҡ
еҢ»зҷӮж©ҹеҷЁгҒ®гғһгӮ№гӮҝгғјгғ•гӮЎгӮӨгғ«зҷ»йҢІгҒ«й–ўгҒҷгӮӢе…¬е‘ҠгҖҒиҮЁеәҠи©ҰйЁ“гӮ¬гӮӨгғүгғ©гӮӨгғігҖҒжҠҖиЎ“жҢҮе°ҺеҺҹеүҮгҒӘгҒ©гӮ’еҗ«гҒҝгҖҒгҒ“гӮҢгӮүгҒ®е…¬е‘ҠгҒЁгӮ¬гӮӨгғүгғ©гӮӨгғігҒҜеҢ»зҷӮж©ҹеҷЁгҒ®з ”究й–ӢзҷәгҖҒзҷ»йҢІгҒЁиІ©еЈІгҒ«е…·дҪ“зҡ„гҒӘж“ҚдҪңжҢҮе°ҺгӮ’жҸҗдҫӣгҒ—гҒҹгҖӮ
- еӣҪгӮ„жҘӯз•ҢгҒ®еҹәжә–пјҡ
еҢ»зҷӮж©ҹеҷЁиЈҪе“ҒгҒҜгҖҒиЈҪе“ҒгҒ®е®үе…ЁжҖ§гҖҒжңүеҠ№жҖ§гҖҒе“ҒиіӘз®ЎзҗҶгҒӘгҒ©гҒ«й–ўйҖЈгҒҷгӮӢеӣҪ家иҰҸж јгӮ„жҘӯз•ҢиҰҸж јгҒ«жә–жӢ гҒҷгӮӢеҝ…иҰҒгҒҢгҒӮгӮӢгҖӮдҫӢгҒҲгҒ°гҖҒGB/T 16886гӮ·гғӘгғјгӮәгҒҜеҢ»зҷӮж©ҹеҷЁгҒ®з”ҹзү©еӯҰзҡ„и©•дҫЎгҒ«й–ўгҒҷгӮӢеӣҪ家жЁҷжә–гҒ§гҒӮгӮӢгҖӮ
- гҖҢеҢ»зҷӮж©ҹеҷЁз”ҹз”Је“ҒиіӘз®ЎзҗҶиҰҸзҜ„гҖҚпјҲGMPпјү
еҢ»зҷӮж©ҹеҷЁгҒ®иЈҪйҖ з®ЎзҗҶеҸҠгҒіе“ҒиіӘз®ЎзҗҶгҒ«й–ўгҒҷгӮӢеҹәжә–пјҲGMPпјүгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгҒ®иЈҪйҖ гҒ«гҒҠгҒ„гҒҰгҖҒиЈҪе“ҒгҒ®е“ҒиіӘгҒ®е®үе®ҡжҖ§еҸҠгҒідҝЎй јжҖ§гӮ’зўәдҝқгҒҷгӮӢгҒҹгӮҒгҒ«еҝ…иҰҒгҒӘе“ҒиіӘз®ЎзҗҶдәӢй …гӮ’е®ҡгӮҒгҒҹгӮӮгҒ®гҒ§гҒӮгӮӢгҖӮ
- гҖҢеҢ»зҷӮж©ҹеҷЁзөҢе–¶е“ҒиіӘз®ЎзҗҶиҰҸзҜ„гҖҚпјҲGSPпјү
еҢ»зҷӮж©ҹеҷЁгҒ®иӘҝйҒ”гҖҒжӨңеҸҺгҖҒдҝқз®ЎгҖҒијёйҖҒгҖҒиІ©еЈІгҒӘгҒ©гҖҒеҢ»зҷӮж©ҹеҷЁжҘӯеӢҷгҒ«гҒҠгҒ‘гӮӢе“ҒиіӘз®ЎзҗҶгҒ«й–ўгҒҷгӮӢиҰҒжұӮдәӢй …гӮ’е®ҡгӮҒгҒҹгӮӮгҒ®гҖӮ
- еҢ»зҷӮж©ҹеҷЁжңүе®ідәӢиұЎгғўгғӢгӮҝгғӘгғігӮ°гҒЁеҶҚи©•дҫЎз®ЎзҗҶејҒжі•
еҢ»зҷӮж©ҹеҷЁжңүе®ідәӢиұЎгғўгғӢгӮҝгғӘгғігӮ°еҸҠгҒіеҶҚи©•дҫЎз®ЎзҗҶејҒжі•гҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгҒ®еёӮиІ©еҫҢжңүе®ідәӢиұЎгҒ®гғўгғӢгӮҝгғӘгғігӮ°гҖҒе ұе‘ҠгҖҒеҲҶжһҗеҸҠгҒіеҮҰзҗҶгҒ®жүӢй ҶгҖҒдёҰгҒігҒ«еҶҚи©•дҫЎгҒ®иҰҒ件гӮ’иҰҸе®ҡгҒ—гҒҰгҒ„гӮӢгҖӮ
- еҢ»зҷӮж©ҹеҷЁиЈҪе“ҒгҒ®зӣЈзқЈз®ЎзҗҶ
еҢ»зҷӮж©ҹеҷЁгҒ®зӣЈзқЈз®ЎзҗҶгҒҜгҖҒгғӘгӮ№гӮҜз®ЎзҗҶгҖҒе…ЁйҒҺзЁӢз®ЎзҗҶгҖҒ科еӯҰзӣЈзқЈгҖҒзӨҫдјҡе…ұеҗҢз®ЎзҗҶгҒ®еҺҹеүҮгҒ«еҫ“гҒЈгҒҰгҒ„гӮӢгҖӮ еӣҪ家гҒҜеҢ»зҷӮж©ҹеҷЁгҒ®еҲҶйЎһз®ЎзҗҶгӮ’е®ҹж–ҪгҒ—гҖҒгғӘгӮ№гӮҜгҒ®зЁӢеәҰгҒ«гӮҲгҒЈгҒҰгҖҒ第дёҖеҲҶйЎһгҒҜдҪҺгғӘгӮ№гӮҜгҖҒ第дәҢеҲҶйЎһгҒҜдёӯгғӘгӮ№гӮҜгҖҒ第дёүеҲҶйЎһгҒҜй«ҳгғӘгӮ№гӮҜгҒ®3гҒӨгҒ«еҲҶйЎһгҒ—гҒҰгҒ„гӮӢгҖӮ гҒқгӮҢгҒһгӮҢгҒ®еҲҶйЎһгҒ«гҒҜгҖҒеҜҫеҝңгҒҷгӮӢз®ЎзҗҶиҰҒ件гҒЁзҷ»йҢІгғ»з”іи«Ӣгғ—гғӯгӮ»гӮ№гҒҢгҒӮгӮӢгҖӮ
- 第дёҖйЎһеҢ»зҷӮж©ҹеҷЁпјҡиЈҪе“ҒеұҠеҮәз®ЎзҗҶгӮ’е®ҹиЎҢгҒҷгӮӢ
- 第дәҢйЎһгҖҒдёүйЎһеҢ»зҷӮж©ҹеҷЁпјҡиЈҪе“Ғзҷ»йҢІз®ЎзҗҶгӮ’е®ҹиЎҢгҒҷгӮӢ
зӣЈзқЈз®ЎзҗҶйғЁй–ҖгҒҜдёӢиЎЁгҒ®йҖҡгӮҠ
| еҲҶйЎһ | 第дёҖйЎһиЈҪе“Ғ | 第дәҢйЎһиЈҪе“Ғ | 第дёүйЎһиЈҪе“Ғ | |
| зҷ»йҢІ | еӣҪз”Ј | еёӮпјҲеёӮе ҙеұҖпјүеұҠеҮә | зңҒпјҲи–¬зӣЈеұҖпјүзҷ»йҢІ | еӣҪ家пјҲи–¬зӣЈеұҖпјүзҷ»йҢІ |
| ијёе…Ҙ | еӣҪ家пјҲи–¬зӣЈеұҖпјүзҷ»йҢІпјҲдёҖйЎһеұҠеҮәпјү | |||
| з”ҹз”Ј | еёӮпјҲеёӮе ҙеұҖпјүеұҠеҮә | зңҒпјҲи–¬зӣЈеұҖпјүиЁұеҸҜ | ||
| зөҢе–¶ | вҖ” | еёӮпјҲеёӮе ҙеұҖпјүеұҠеҮә | еёӮпјҲеёӮе ҙеұҖпјүиЁұеҸҜ | |
В
- еҢ»зҷӮж©ҹеҷЁиЈҪе“ҒгҒ®еұҠеҮәпјҸзҷ»йҢІгғ—гғӯгӮ»гӮ№
еӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҜгҖҒеҢ»зҷӮж©ҹеҷЁгҒ®е®үе…ЁжҖ§гҖҒжңүеҠ№жҖ§гҖҒе“ҒиіӘгӮ’зўәдҝқгҒҷгӮӢгҒҹгӮҒгҒ«гҖҒеҢ»зҷӮж©ҹеҷЁиЈҪе“ҒгҒ®з”іи«Ӣгғ»зҷ»йҢІгғ—гғӯгӮ»гӮ№гӮ’з®ЎзҗҶгҒ—гҖҒдёҖйҖЈгҒ®жүӢз¶ҡгҒҚгҒЁиҰҒ件гӮ’жәҖгҒҹгҒҷгҒ“гҒЁгҒҢгҒ§гҒҚгӮӢгҖӮ
в‘ гҖҖдёӯеӣҪгҒ«гҒҠгҒ‘гӮӢ第дёҖйЎһеҢ»зҷӮж©ҹеҷЁеұҠеҮә
- еұҠеҮәжғ…е ұгҒ®жҸҗеҮәпјҡеұҠеҮәдәәгҒҜгҖҒеұҠеҮәжғ…е ұгӮ’еҪ“и©Іең°еҢәгҒ®и–¬зү©зӣЈзқЈз®ЎзҗҶгӮ’жӢ…еҪ“гҒҷгӮӢеёӮгҒ®жӢ…еҪ“йғЁзҪІгҒ«жҸҗеҮәгҒҷгӮӢгҖӮ
- еҮәйЎҳз•ӘеҸ·гҒ®еҸ–еҫ—пјҡзӣЈзқЈз®ЎзҗҶйғЁй–ҖгҒҜжҸҗеҮәгҒ•гӮҢгҒҹеұҠеҮәиіҮж–ҷгӮ’дҝқеӯҳгҒ—гҖҒеұҠеҮәз•ӘеҸ·гӮ’д»ҳдёҺгҒҷгӮӢгҖӮ
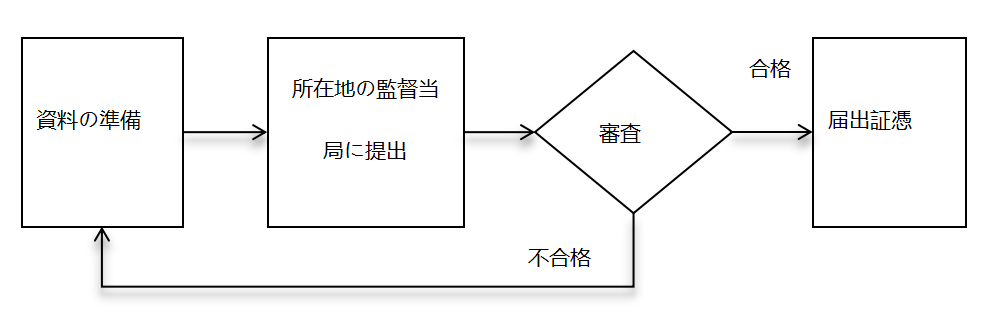
в‘ЎгҖҖијёе…Ҙ第дёҖйЎһеҢ»зҷӮж©ҹеҷЁеұҠеҮә
- еұҠеҮәиіҮж–ҷгҒ®жҸҗеҮәпјҡеұҠеҮәдәәгҒҜеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒ«еұҠеҮәиіҮж–ҷгӮ’жҸҗеҮәгҒҷгӮӢгҖӮ
- еұҠеҮәз•ӘеҸ·гҒ®еҸ–еҫ—пјҡеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҜжҸҗеҮәгҒ•гӮҢгҒҹеұҠеҮәиіҮж–ҷгӮ’дҝқеӯҳгҒ—гҖҒеұҠеҮәз•ӘеҸ·гӮ’д»ҳдёҺгҒҷгӮӢгҖӮ
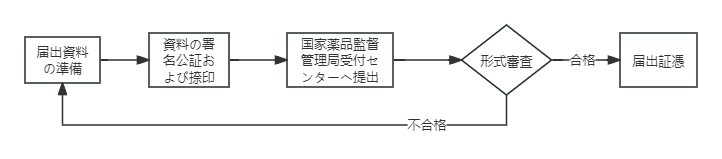
в‘ўгҖҖдёӯеӣҪеӣҪеҶ…第дәҢйЎһгҖҒ第дёүйЎһеҢ»зҷӮж©ҹеҷЁзҷ»йҢІ
- зҷ»йҢІз”іи«ӢгҒ®жҸҗеҮәпјҡз”іи«ӢиҖ…гҒҜзңҒгҖҒиҮӘжІ»еҢәгҖҒеёӮзӣҙиҪ„гҒ®и–¬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҫгҒҹгҒҜеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒ«зҷ»йҢІз”іи«ӢжӣёгӮ’жҸҗеҮәгҒҷгӮӢгҖӮ
- еҜ©жҹ»пјҡй–ўйҖЈйғЁй–ҖгҒҢз”іи«ӢиіҮж–ҷгӮ’еҜ©жҹ»гҒҷгӮӢгҖӮ
- жүҝиӘҚпјҡеҜ©жҹ»еҗҲж јеҫҢгҖҒеҢ»зҷӮж©ҹеҷЁзҷ»йҢІиЁјгҒҢзҷәиЎҢгҒ•гӮҢгӮӢгҖӮ
в‘ЈгҖҖијёе…Ҙ第дәҢйЎһгҖҒ第дёүйЎһеҢ»зҷӮж©ҹеҷЁзҷ»йҢІ
- зҷ»йҢІз”іи«ӢгҒ®жҸҗеҮәпјҡз”іи«ӢиҖ…гҒҜеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒ«зҷ»йҢІз”іи«ӢгӮ’жҸҗеҮәгҒҷгӮӢгҖӮ
- еҜ©жҹ»пјҡеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶеұҖгҒҜз”іи«ӢжӣёйЎһгӮ’еҜ©жҹ»гҒҷгӮӢгҖӮ
- жүҝиӘҚпјҡеҜ©жҹ»йҖҡйҒҺеҫҢгҖҒеҢ»зҷӮж©ҹеҷЁзҷ»йҢІиЁјгӮ’зҷәиЎҢгҒҷгӮӢгҖӮ
дәҢйЎһ/дёүйЎһеҢ»зҷӮж©ҹеҷЁиЈҪе“Ғзҷ»йҢІгғ—гғӯгӮ»гӮ№
В
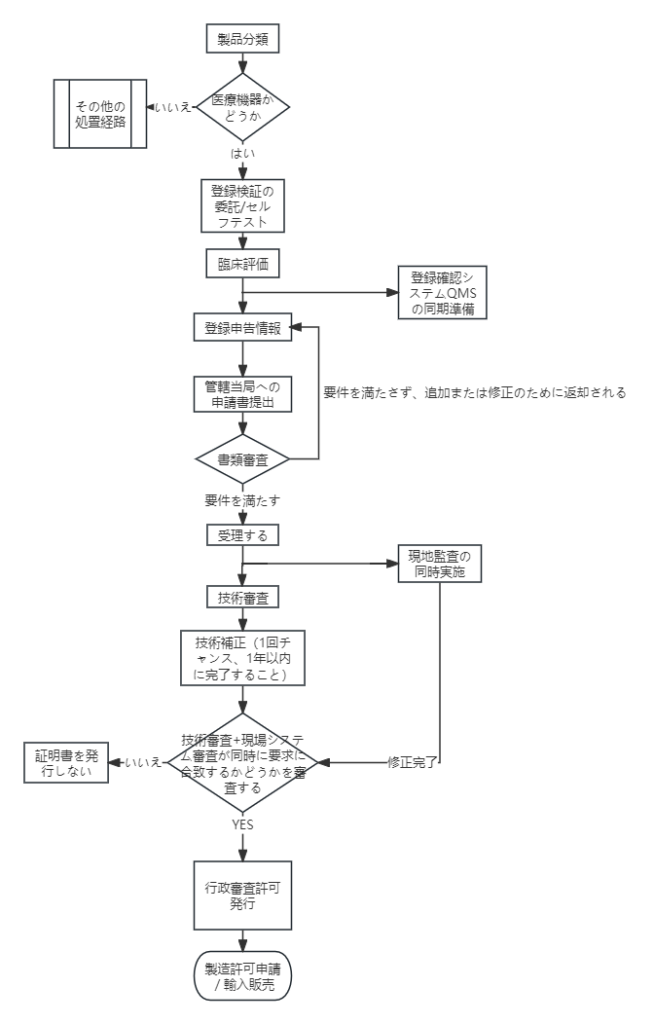
В
- гӮөгғјгғ“гӮ№еҶ…е®№
- еӣҪеҶ…еҢ»зҷӮж©ҹеҷЁиЈҪе“ҒеұҠеҮә/зҷ»йҢІгӮөгғјгғ“гӮ№

- жө·еӨ–еҢ»зҷӮж©ҹеҷЁиЈҪе“ҒеұҠеҮәгғ»зҷ»йҢІгӮөгғјгғ“гӮ№
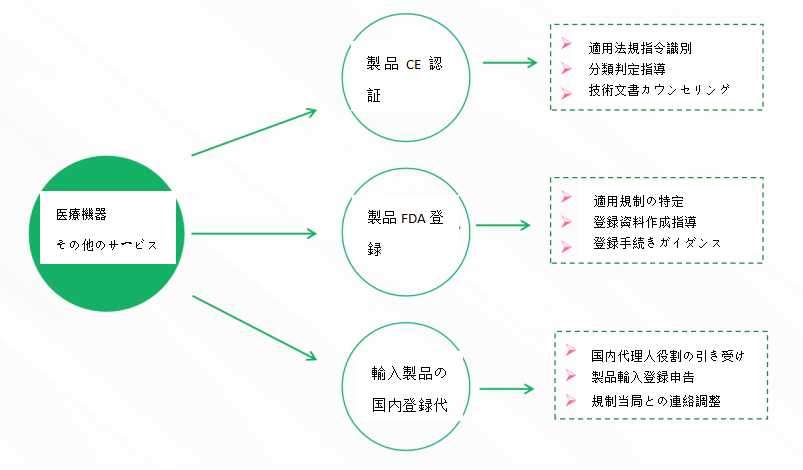
- еҢ»зҷӮж©ҹеҷЁиҮЁеәҠи©•дҫЎгӮөгғјгғ“гӮ№
| еҢ»зҷӮж©ҹеҷЁиҮЁеәҠи©•дҫЎгӮөгғјгғ“гӮ№ | иҮЁеәҠи©ҰйЁ“жҢҮе°ҺгӮөгғјгғ“гӮ№ | жІ»йЁ“е®ҹж–ҪиЁҲз”»жӣёгҒ®дҪңжҲҗгғ»и©•дҫЎ |
| жІ»йЁ“е®ҹж–ҪеҢ»зҷӮж©ҹй–ўгҒ®иӘҝжҹ»гғ»еҜ©жҹ» | ||
| жІ»йЁ“гғ—гғӯгӮёгӮ§гӮҜгғҲй–Ӣе§ӢпјҲгғ—гғӯгӮёгӮ§гӮҜгғҲз”іи«ӢгҖҒеҖ«зҗҶеҜ©жҹ»гҖҒжІ»йЁ“з”іи«ӢгҖҒеҘ‘зҙ„з· зөҗгҖҒй–Ӣе§Ӣдјҡиӯ°пјү | ||
| жІ»йЁ“йҒәдјқеӯҗдәӢеӢҷеұҖжүҝиӘҚз”іи«ӢгӮігғігӮөгғ«гғҶгӮЈгғігӮ°жҘӯеӢҷ | ||
| жІ»йЁ“гғўгғӢгӮҝгғӘгғігӮ°жҘӯеӢҷ | ||
| иҮЁеәҠи©ҰйЁ“е“ҒиіӘзӣЈжҹ» | ||
| жІ»йЁ“гғҮгғјгӮҝз®ЎзҗҶ | ||
| иҮЁеәҠи©ҰйЁ“зөұиЁҲеҲҶжһҗ | ||
| иҮЁеәҠи©ҰйЁ“е ұе‘ҠжӣёдҪңжҲҗгҖҒгғ¬гғ“гғҘгғјгҖҒдҝ®жӯЈ | ||
| еҗҢзЁ®жҜ”ијғиҮЁеәҠи©•дҫЎ | иҮЁеәҠи©•дҫЎгӮігғігӮөгғ«гғҶгӮЈгғігӮ°пјҲеҗҢзЁ®иЈҪе“ҒжҜ”ијғпјү | |
| е…ҚйҷӨиҮЁеәҠжҜ”ијғиӘ¬жҳҺпјҲе…ҚйҷӨиҮЁеәҠи©ҰйЁ“гӮ«гӮҝгғӯгӮ°гҒ®иЈҪе“ҒгҒ«гҒӨгҒ„гҒҰпјү |
1.еҢ»зҷӮж©ҹеҷЁе“ҒиіӘгғһгғҚгӮёгғЎгғігғҲгӮ·гӮ№гғҶгғ гҒ®з”ұжқҘ
е“ҒиіӘз®ЎзҗҶгӮ·гӮ№гғҶгғ пјҲQuality Management SystemгҖҒQMSпјүгҒЁгҒҜгҖҒе“ҒиіӘгҒ®йқўгҒ§зө„з№”гӮ’жҢҮжҸ®гғ»еҲ¶еҫЎгҒҷгӮӢз®ЎзҗҶгӮ·гӮ№гғҶгғ гӮ’жҢҮгҒҷгҖӮQMSгҒҜгҖҒиЈҪе“ҒгӮ„гӮөгғјгғ“гӮ№гҒ®е“ҒиіӘгҒҢйЎ§е®ўгҒ®жңҹеҫ…гҒЁгғӢгғјгӮәгҒ«еҗҲгҒЈгҒҰгҒ„гӮӢгҒ“гҒЁгӮ’дҝқиЁјгҒҷгӮӢгҒҹгӮҒгҒ®зө„з№”зҡ„гҒӘж–№жі•гҒ§гҒҷгҖӮQMSгҒ®дё»гҒӘзӣ®жЁҷгҒҜгҖҒиЈҪе“ҒгҒҫгҒҹгҒҜгӮөгғјгғ“гӮ№гҒ®дёҖиІ«жҖ§гҒЁдҝЎй јжҖ§гӮ’зўәдҝқгҒ—гҖҒйЎ§е®ўгҒ®жңҹеҫ…гҒЁгғӢгғјгӮәгӮ’жңҖеӨ§йҷҗгҒ«жәҖгҒҹгҒҷгҒ“гҒЁгҒ§гҒӮгӮӢгҖӮ
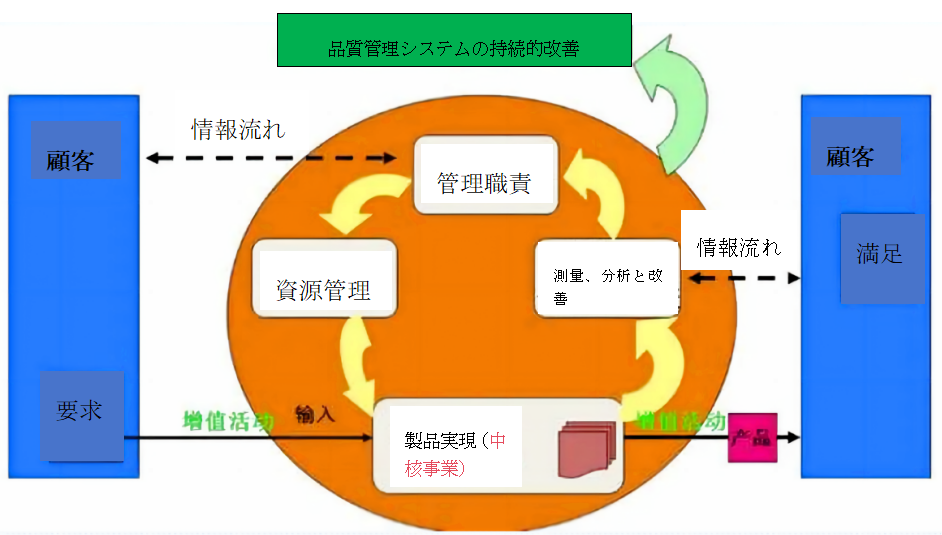
2.еҢ»зҷӮж©ҹеҷЁжҘӯз•ҢгҒ«гҒҠгҒ‘гӮӢе“ҒиіӘгғһгғҚгӮёгғЎгғігғҲгӮ·гӮ№гғҶгғ иҰҒ件
еҢ»зҷӮж©ҹеҷЁжҘӯз•ҢгҒ®иЈҪе“Ғе“ҒиіӘгғӘгӮ№гӮҜгҒҜдәәгҒ®з”ҹе‘ҪеҒҘеә·гҒЁеҜҶжҺҘгҒ«й–ўйҖЈгҒ—гҒҰгҒҠгӮҠгҖҒиЈҪе“Ғе“ҒиіӘгҒ®зӣЈзқЈз®ЎзҗҶгҒ«гҒҜеҗ„еӣҪгҒ®жі•иҰҸеҹәжә–гӮ’еҹәзӨҺгҒЁгҒҷгӮӢеҝ…иҰҒгҒҢгҒӮгӮӢгҒҹгӮҒгҖҒISO9001гӮ’еҹәзӨҺгҒЁгҒ—гҒҰISO13485пјҲGB/T 42061пјүеҢ»зҷӮж©ҹеҷЁе“ҒиіӘз®ЎзҗҶгӮ·гӮ№гғҶгғ гӮ’жі•иҰҸгҒ®иҰҒжұӮгҒ«з”ЁгҒ„гӮӢгҒҹгӮҒгҒ®е°Ӯз”ЁQMSеҹәжә–гӮ’еҲ¶е®ҡгҒ—гҒҹгҖӮ
дёӯеӣҪеӣҪ家薬е“ҒзӣЈзқЈз®ЎзҗҶз·ҸеұҖгҒҜгҖҒгӮҲгӮҠзӣҙж„ҹзҡ„гҒ§жҢҮе°Һзҡ„гҒӘгӮӮгҒ®гҒ«гҒҷгӮӢгҒҹгӮҒгҖҒеҢ»зҷӮж©ҹеҷЁиЈҪйҖ жҘӯиҖ…гҒ®е“ҒиіӘз®ЎзҗҶгӮ·гӮ№гғҶгғ ж§ӢзҜүгҒЁз¶ӯжҢҒгҒ®гҒҹгӮҒгҒ®еҢ»зҷӮж©ҹеҷЁд»•ж§ҳжӣёдёҖејҸгӮ’еҲ¶е®ҡгҒ—гҒҹгҖӮ
- GB/TвҖӮ42061-2022еҢ»зҷӮж©ҹеҷЁе“ҒиіӘз®ЎзҗҶгӮ·гӮ№гғҶгғ иҰҸеҲ¶иҰҒжұӮдәӢй …з”Ё
- еҢ»зҷӮж©ҹеҷЁз”ҹз”Је“ҒиіӘз®ЎзҗҶиҰҸзҜ„зҸҫе ҙжӨңжҹ»жҢҮе°ҺеҺҹеүҮ
- еҢ»зҷӮж©ҹеҷЁгҒ®з”ҹз”Је“ҒиіӘз®ЎзҗҶиҰҸзҜ„з„ЎиҸҢеҢ»зҷӮж©ҹеҷЁгҒ®зҸҫе ҙжӨңжҹ»жҢҮе°ҺеҺҹеүҮ
- еҢ»зҷӮж©ҹеҷЁиЈҪйҖ е“ҒиіӘз®ЎзҗҶеҹәжә–жӨҚиҫјгҒҝеһӢеҢ»зҷӮж©ҹеҷЁзҸҫе ҙжӨңжҹ»жҢҮйҮқ
- еҢ»зҷӮж©ҹеҷЁз”ҹз”Је“ҒиіӘз®ЎзҗҶиҰҸзҜ„дҪ“еӨ–иЁәж–ӯи©Ұи–¬гҒ®зҸҫе ҙжӨңжҹ»жҢҮе°ҺеҺҹеүҮ
- еҢ»зҷӮж©ҹеҷЁиЈҪйҖ з®ЎзҗҶгҒҠгӮҲгҒіе“ҒиіӘз®ЎзҗҶеҹәжә–гҒ«гҒҠгҒ‘гӮӢгӮ«гӮ№гӮҝгғ гғЎгӮӨгғүзҫ©жӯҜгҒ®зҸҫе ҙжӨңжҹ»гӮ¬гӮӨгғүгғ©гӮӨгғі
- еҢ»зҷӮж©ҹеҷЁз”ҹз”Је“ҒиіӘз®ЎзҗҶиҰҸзҜ„зӢ¬з«ӢгӮҪгғ•гғҲгӮҰгӮ§гӮўзҸҫе ҙжӨңжҹ»жҢҮе°ҺеҺҹеүҮ
- еҢ»зҷӮж©ҹеҷЁзҷ»йҢІе“ҒиіӘгғһгғҚгӮёгғЎгғігғҲгӮ·гӮ№гғҶгғ жӨңиЁјгӮ¬гӮӨгғүгғ©гӮӨгғі
- еҢ»зҷӮж©ҹеҷЁдәӢжҘӯе“ҒиіӘз®ЎзҗҶеҹәжә–
- еҢ»зҷӮж©ҹеҷЁијёйҖҒгғ»дҝқз®ЎгӮөгғјгғ“гӮ№е°Ӯй–ҖдјҒжҘӯгҒ®е“ҒиіӘз®ЎзҗҶгҒ«й–ўгҒҷгӮӢз«Ӣе…ҘжӨңжҹ»гӮ¬гӮӨгғүгғ©гӮӨгғі
3.гӮөгғјгғ“гӮ№еҶ…е®№
еҢ»зҷӮж©ҹеҷЁжҘӯз•ҢгҒ«гҒҠгҒ‘гӮӢQMSгҒҜгҖҒиЈҪе“ҒиЁӯиЁҲгғ»й–ӢзҷәгғӘгӮ№гӮҜз®ЎзҗҶгҖҒз”ҹз”Је·ҘзЁӢз®ЎзҗҶгҖҒе“ҒиіӘз®ЎзҗҶгҖҒиҮӘдё»жӨңжҹ»з®ЎзҗҶгҖҒиҮЁеәҠи©•дҫЎгҖҒжңүе®ідәӢиұЎгғ»еҶҚи©•дҫЎз®ЎзҗҶгҖҒUDIгӮ·гӮ№гғҶгғ з®ЎзҗҶгҖҒ委託з”ҹз”ЈзӣЈзқЈз®ЎзҗҶгҖҒеёӮиІ©еҫҢзӣЈзқЈгӮ’зөұеҗҲгҒ—гҒҹгҖҒжі•иҰҸгҒ«еҹәгҒҘгҒҸеёӮиІ©еүҚгҒЁеёӮиІ©еҫҢгҒ®дёЎж®өйҡҺгӮ’гӮ«гғҗгғјгҒҷгӮӢгғ•гғ«гғ©гӮӨгғ•гӮөгӮӨгӮҜгғ«гғһгғҚгӮёгғЎгғігғҲгӮ·гӮ№гғҶгғ гҒ§гҒӮгӮӢгҖӮ
ж–°е®үжҪӨгҒҜгҒҠе®ўж§ҳгҒ«д»ҘдёӢгҒ®е“ҒиіӘз®ЎзҗҶгӮ·гӮ№гғҶгғ йҒ©з”Ёжі•иҰҸиӯҳеҲҘгҖҒгӮ·гӮ№гғҶгғ жһ зө„гҒҝж§ӢзҜүгҖҒгӮ·гӮ№гғҶгғ ж–ҮжӣёдҪңжҲҗжҢҮе°ҺгҖҒгӮ·гӮ№гғҶгғ йҒӢз”ЁзӣЈжҹ»иЁәж–ӯгҖҒ第дёүиҖ…зӣЈжҹ»еҜҫеҝңзӣёи«ҮгҒӘгҒ©гҒ®гӮөгғјгғ“гӮ№гӮ’жҸҗдҫӣгҒ—гҒҰгҒ„гӮӢгҖӮ


WeChatе…¬ејҸгӮўгӮ«гӮҰгғігғҲ
еҢ–еӯҰе“Ғ法规еүҚжІҝ

 дёӯж–Ү
дёӯж–Ү English
English